Abertas pela Agência Nacional de Vigilância Sanitária (Anvisa) e recebendo participações até 7 de dezembro, duas consultas públicas preocupam a medicina diagnóstica brasileira. As CPS 911 e 912 visam promover modificações no segmento liberando a realização de exames laboratoriais em farmácias e drogarias, denominando esses estabelecimentos como Serviços de Apoio ao Diagnóstico e Terapêutico que realizam Testes de Análises Clínicas (SADT-TAC). Porém, especialistas da LAS (Laboratórios Associados) apontam que os riscos dessa abertura são muito maiores do que os benefícios.
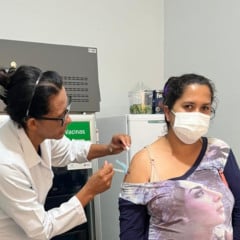
Hoje, farmácias e drogarias estão autorizadas a realizar apenas testes rápidos para glicose e para covid-19. Também chamados de point-of-care testing (POCT) ou de testes laboratoriais remotos (TLR), são dispositivos feitos para serem utilizados fora do ambiente laboratorial, justamente por isso são mecanismos adotados em serviços hospitalares de pronto-atendimento, por exemplo.
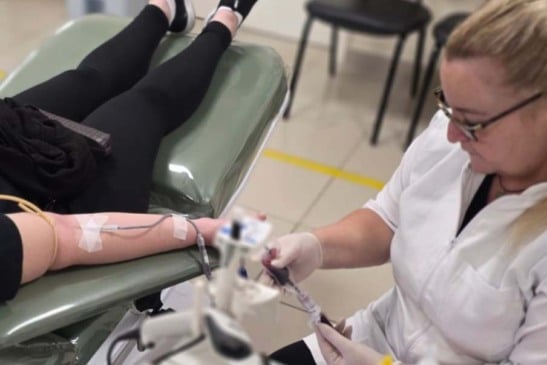
Porém, segundo explicado pela LAS, caso as consultas públicas avancem da forma como estão sendo apresentadas, além de liberar a realização de qualquer TLR em farmácias e drogarias independentemente de sua complexidade – pois existem testes laboratoriais remotos de alta complexidade envolvendo inclusive biologia molecular – os textos abrem brechas para que esses estabelecimentos possam, inclusive, realizar a coleta de amostras, despachando-as para laboratórios de apoio.
“Não podemos tratar os serviços de saúde como se fossem produtos, pois isso banaliza um atendimento que precisa estar fundamentado em rígidas diretrizes para garantir a segurança dos pacientes. Permitir que estabelecimentos prioritariamente comerciais atuem como estabelecimentos de saúde não traz ganhos e o principal prejudicado é o paciente”, explica Jorge Alberto Schaefer, farmacêutico-bioquímico, analista clínico e membro da diretoria do LAS.
De acordo com o grupo, a modificação de nomenclaturas – já que as consultas públicas passam a chamar os exames de testes – podem agir como uma minimização da complexidade do serviço, o que não é válido e soa como mais um risco à segurança dos pacientes.
Para Schaefer, os textos das CPs 911 e 912 ignoram inclusive legislações mundiais do setor, como é o caso da ISO 15.189, norma utilizada pelos laboratórios clínicos para confirmação ou reconhecimento de suas competências. “O principal ponto está na qualidade dos resultados que serão gerados por meio desses exames feitos sem qualquer suporte de profissionais altamente especializados em todas as etapas desse serviço. Se a proposta não traz qualidade e não traz segurança para o paciente, por que estamos tratando desse assunto?”, questiona o especialista que também se preocupa com a fiscalização, que exigirá a contratação de mais fiscais e a qualificação desses profissionais para que possam de fato compreender se as diretrizes estão sendo seguidas.
Na visão da LAS, o importante é que a sociedade civil compreenda, com transparência, o que está sendo proposto. E que saiba, inclusive, que os testes rápidos são alvo de muitos questionamentos de confiabilidade, o que pode ser observado recentemente durante a pandemia de covid-19 quando esses testes remotos passaram a entregar muitos resultados tanto falso positivos quanto falso negativos. “Não se pode criar uma imagem, para o consumidor, de que as farmácias terão todos os recursos que têm os laboratórios clínicos. A Anvisa, inclusive, precisa comunicar à população quais testes têm baixa sensibilidade, quais são confiáveis, e quais não são. Precisamos investir cada vez mais na qualidade e segurança do paciente, e não o contrário”, finaliza Schaefer.
SOBRE O LAS
A LAS – Laboratórios Associados é uma rede de cooperação pioneira entre laboratórios de medicina diagnóstica, presentes em diversas cidades do Rio Grande do Sul, Santa Catarina e Paraná. Tem como objetivo, fortalecer e qualificar os diversos laboratórios associados através de uma busca constante por conhecimento técnico, troca de experiências e acesso a novas tecnologias.